多措并举鼓励创新 儿童药审评审批继续保持增长势头
目前,国家药监局组织修订的《中华人民共和国药品管理法实施条例(修订草案征求意见稿)》正在挂网公开征求意见,其中提出“对首个批准上市的儿童专用新品种、剂型和规格,以及增加儿童适应症或者用法用量的,给予最长不超过12个月的市场独占期,期间内不再批准相同品种上市。” 征求意见稿对于企业研发儿童用药给出了实质性激励条款,但并非唯一激励政策。记者了解到,为切实解决儿童用药保障及药品质量安全问题,近年来国家药监局多措并举,鼓励研发、提升审评效率,健全工作机制,多方谋划解决儿童用药研发重点、难点问题,鼓励和促进儿童用药的研发创新,不断满足临床需求,全面提高我国儿童用药的可获得性和安全性。据悉,截至2022年4月30日,国家药监局药审中心已完成30件儿童用药技术审评任务,共计21个品种,其中包含8个优先审评审批品种和3个《鼓励研发申报儿童药品清单》品种。
儿童要用儿童药
通常,儿童用药是指适合18岁以下未成年人的一类药品。由于儿童的生理功能特殊,尤其是肝、肾、神经和内分泌功能发育不全,其在药物吸收、分布、代谢等有特殊规律,并不是成人的缩小版,儿童药品在剂量、安全性、口味等都有特殊的需求。随着经济水平的提升,国家生育政策的放开,儿童人口数量持续增加,儿童用药需求也在不断提升。但长期以来,我国儿童药物处于专用品种少、适宜剂型少、生产企业少的局面。究其原因,儿童用药的研发和生产,受伦理、临床试验可行性、产业政策和市场等多方面因素影响,其可获得性和安全性的保障难度远高于成人用药。
具体来说,一是从新药研发上看,由于儿童人群的特殊性,在剂型设计、规格选择、安全性评估临床试验的设计等方面存在困难,不能完全适用已发布的成人药品研发技术指导原则。二是从已上市的药品看,现有可用于儿童的药品,其说明书普遍存在用药信息不规范或数据缺失等情况,制约了儿童用药。三是从管理上看,儿童用药研发本身难度较大、不确定性强,业界研发积极性不高。
此前,国家药监局药审中心发布的《中国新药注册临床试验现状年度报告(2020年)》显示:儿童受试者的临床试验为129项,占当年登记的药物临床试验总数的8.8%,仅在儿童人群中开展的新药临床试验共登记33项,仅占新药临床试验总体的2.2%。
“儿科药物受试者招募困难、安全性风险高,导致临床试验周期长、研发风险高,费用高。”业内人士告诉记者,愿意让孩子参与临床试验的父母凤毛麟角,加之与幼龄儿童进行身体感受的沟通表达等困难,致使儿科药物临床试验数量较少,而罕见病药物的试验对象招募则更加艰难。
在上述报告中,登记的129项目儿科临床试验,按药物分类分析,生物制品登记数量最多,为70项,其次为化学药和中药;按适应症分析,主要适应症领域分布为抗肿瘤药物、预防性疫苗、皮肤和五官科等,生物制品和化学药主要适应症分布大致相同,中药主要为呼吸类药物。据介绍,在儿童药领域,还有太多临床未被满足的需求,除了药物的有效性和安全性,适合儿童的给药方式,药品口味等都存在更多的提升空间。
儿童药研发审评审批快车道
2011年,我国开始明确鼓励儿童专用药品研发生产,完善儿童用药目录。围绕解决儿童用药研发重点难点问题,近年来,国家药监局推出鼓励研发创新、提升审评效率、改进工作作风、保障药品安全的“组合拳”措施。
2016年,药审中心发布了《关于临床急需儿童用药申请优先审评审批品种评定基本原则及首批优先审评品种的公告》,首批5个儿童用药注册申请获得优先审评审批。
2019年,新修订的《药品管理法》明确鼓励儿童用药的研制和创新,支持开发符合儿童生理特征的儿童用药新品种、剂型和规格,对儿童用药予以优先审评审批。
2020年新修订的《药品注册管理办法》加快上市注册程序中设立优先审评通道,将儿童用药品纳入到优先审评审批程序。
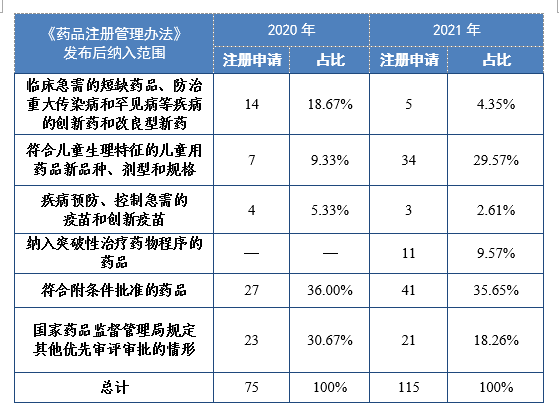
数据来源:2021年度药品审评报告
那么,这个优先审评究竟能有多快呢?
据药审中心介绍,与一般申报路径相比,优先审评审批程序缩短至130个工作日,临床急需境外新药审评时限为70个工作日,药审中心在审评系统中设立“儿童用药”特殊标识,由项目管理人专人对接,督导审评进度,确保各项环节按时推进、无缝衔接,通过多方优化审评资源配置,加快儿童用药上市。
近年来,我国已先后加快审批治疗5q脊髓性肌萎缩症的诺西那生钠注射液、治疗法布雷病的阿加糖酶α注射用浓溶液等16个儿童用药获批上市,为提高患儿生存率和生活质量带来了新的希望。
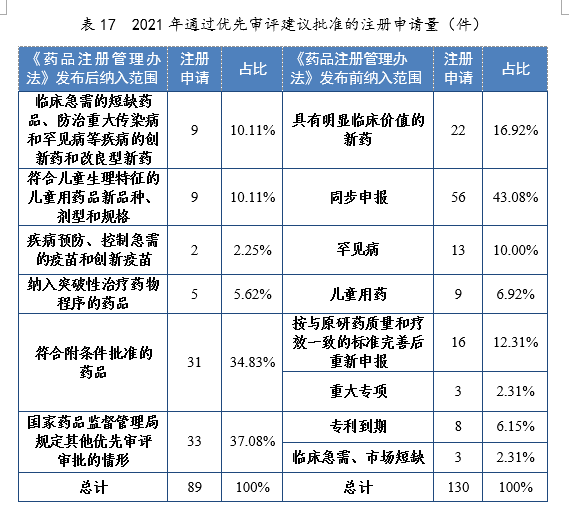
数据来源:2021年度药品审评报告
组合拳加快儿童用药上市机制
针对企业开展儿童用药研发痛点难点问题,国家药监局加强研究、对症下药,对儿童用药适用规格、剂型缺乏等问题深入调研,按照“急用先行”的原则,结合临床实际建立包括成人用药数据外推、真实世界数据支持等指导原则在内的儿童用药研发审评证据体系。截至2021年底,共发布《儿童用药(化学药品)药学开发指导原则(试行)》等12项儿童用药专项指导原则,完善了儿童用药临床试验和安全性评价标准,为研发和审评提供了重要技术支持与审评依据,激发了企业研发活力。2022年,已将4项儿童用药专项指导原则列入年度工作计划。
为加快境外已上市药品进入中国,满足我国临床需求,国家药监局会同国家卫健委组织专家遴选并发布临床急需境外新药品种目录,对于纳入品种加大服务指导力度,动员企业来中国申报,对申报品种建立专门通道开展审评,共发布三批临床急需境外新药品种目录。
此外,为切实了解儿童用药临床需求,加强对企业研发工作的支持,国家药监局加强与各有关部门、国家儿童医学中心及产业界在儿童药物研发领域的合作,召开儿童用药研发相关政策及技术指导原则研讨会,作为指导单位派员参与中国儿童用药研发与产业化联盟相关研讨,赴国家儿童医学中心开展实地调研,进一步对接临床需求,针对企业研发中的实际困难予以指导,建立解决儿童用药研发的协同合作机制,共同促进儿童用药创新研发。
针对临床机构反映的儿童患者超说明书使用药品问题,国家药监局药审中心与国家儿童医学中心签署战略合作协议,设立“中国儿童说明书规范化项目”,开展已上市药品说明书中儿童用药信息的规范化增补工作。国家药监局创新监管手段,以儿科临床需求为导向,在充分论证基础上,采用前沿的研究方法,基于儿科临床实际用药数据,以遵重科学性确保安全性为前提合理利用真实世界证据,对已上市药品说明书增加儿童用药信息,指导临床合理安全用药。
在多重政策激励下,在2021年全年,我国共计有47个儿童用药获得上市批准,其中,包括儿科吸入制剂、轮状病毒疫苗、中药颗粒剂等重要品种和剂型,儿童用药的申报与审批数量正呈现稳步上升趋势。
——来源于医药经济报